



























Estude fácil! Tem muito documento disponível na Docsity

Ganhe pontos ajudando outros esrudantes ou compre um plano Premium


Prepare-se para as provas
Estude fácil! Tem muito documento disponível na Docsity
Prepare-se para as provas com trabalhos de outros alunos como você, aqui na Docsity
Os melhores documentos à venda: Trabalhos de alunos formados
Prepare-se com as videoaulas e exercícios resolvidos criados a partir da grade da sua Universidade
Responda perguntas de provas passadas e avalie sua preparação.

Ganhe pontos para baixar
Ganhe pontos ajudando outros esrudantes ou compre um plano Premium
Comunidade
Peça ajuda à comunidade e tire suas dúvidas relacionadas ao estudo
Descubra as melhores universidades em seu país de acordo com os usuários da Docsity
Guias grátis
Baixe gratuitamente nossos guias de estudo, métodos para diminuir a ansiedade, dicas de TCC preparadas pelos professores da Docsity
Neste documento, aprenda sobre a história do descobrimento da estrutura atômica, começando pelas primeiras teorias atômicas dos gregos antigos, passando pelas descobertas de john dalton e os raios catódicos e elétrons, até os experimentos clássicos de millikan e rutherford. Explore as teorias atômicas, a natureza ondulatória da luz e a estrutura atômica moderna.
O que você vai aprender
Tipologia: Notas de estudo
1 / 35

Esta página não é visível na pré-visualização
Não perca as partes importantes!




























Verifica-se que, permanecendo constante a massa de nitrogênio, as massas de oxigênio apresentam, entre si, uma relação simples de números inteiros e pequenos, ou seja, 1:2:3:4:.
A descoberta da estrutura
atômica
A descoberta da estrutura atômica
https://www.youtube.com/watch?v=XU8nMKkzbT
Experimento da gota de óleo – Millikan
A descoberta da estrutura atômica
Experimento da gota de óleo - Millikan
A descoberta da estrutura atômica
A descoberta da estrutura
atômica
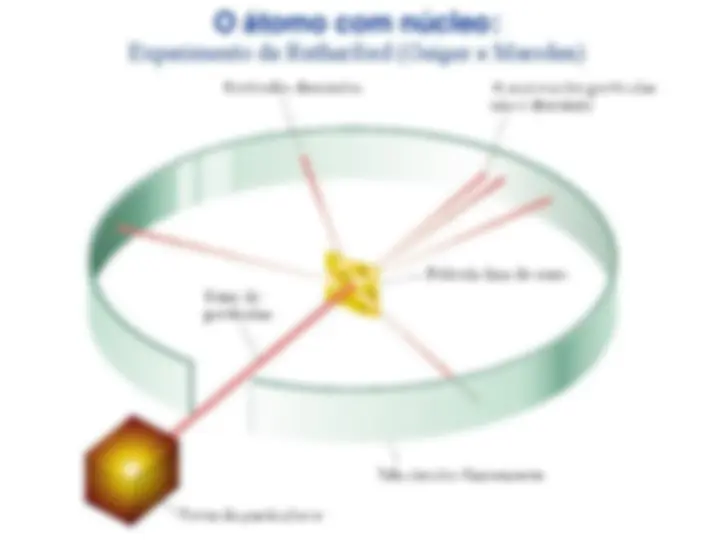
Experimento de Rutherford (Geiger e Marsden)
A descoberta da estrutura atômica
A descoberta da estrutura
atômica
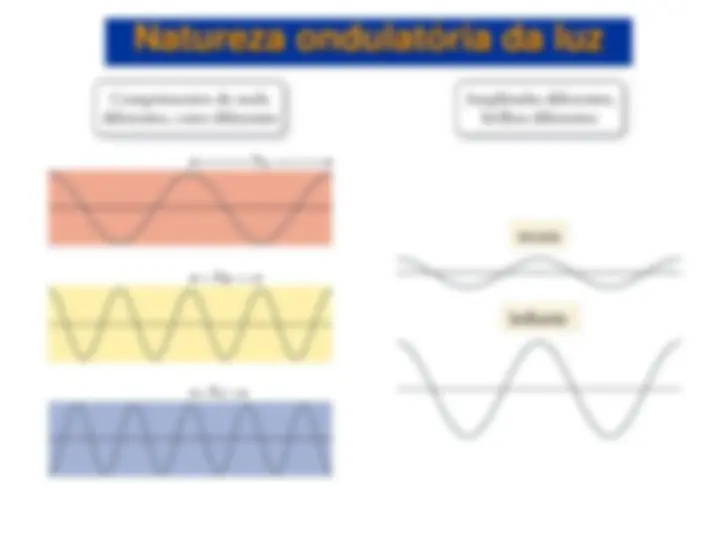
Elétrons em átomos
Elétrons em átomos